flowchart TD
A[开始:评估化学品] --> B[收集UV/vis吸收数据<br/>290-700 nm范围]
B --> C{MEC > 1000 L mol⁻¹ cm⁻¹?}
C -->|否| D[无需光毒性测试<br/>无光毒性潜力]
C -->|是| E[进行体外3T3 NRU光毒性测试]
E --> F{检查测试局限性}
F --> G[考虑代谢激活需求]
F --> H[检查溶解度和稳定性]
F --> I[评估是否为混合物]
G --> J[执行测试<br/>记录所有观察]
H --> J
I --> J
J --> K[计算PIF和MPE]
K --> L{PIF > 5 或 MPE > 0.15?}
L -->|是| M[光毒性阳性]
L -->|否| N{PIF < 2 或 MPE < 0.1?}
N -->|是| O[光毒性阴性]
N -->|否| P[结果不确定<br/>考虑补充测试]
体外3T3 NRU光毒性测试标准操作程序 (SOP)
OECD 测试指南 432
测试方法介绍
方法验证历史与背景
本测试方法是经正式验证的体外方法,用于评估化学品的光细胞毒性。
验证状态
该方法是欧盟替代方法验证中心(ECVAM)于1995-1998年间协调进行的国际验证研究的成果。验证过程遵循OECD系列测试与评估文件No. 34所述的原则。
方法发展历程
- 1995年:该方法基于CVMP/EU/CVMP/032/95文件首次通过
- 1996-1998年:进行全面的实验室间验证研究
- 2000年:被欧盟批准为化妆品成分光毒性筛选的替代方法
- 2004年:首次被OECD采纳为测试指南432
- 2019年:最新版本更新,进一步明确了接受标准和决策标准
与其他验证方法的关系
| 方法 | 全称 | 主要应用 |
|---|---|---|
| 3T3 NRU PT | 3T3细胞中性红摄取光毒性测试 | 细胞活力测试(本方法) |
| RSM | 红细胞光溶血测试 | 红细胞膜光损伤评估 |
| 3T3 NRU PT + RSM | 组合策略 | 提高预测准确性的整合方法 |
验证研究结论
- 高预测能力:敏感性≥95%,特异性≥80%
- 良好的重现性:实验室间变异系数低
- 广泛的适用性:适用于多种化学类别
- 动物福利优势:完全替代动物进行的光毒性测试
概述
目的
本标准操作程序(SOP)描述了体外3T3中性红摄取(NRU)光毒性测试方法,用于:
- 识别经光激活的受试化学品的光毒性潜力
- 评估化学品在光照和非光照条件下的细胞毒性差异
- 预测化学品在体内的光毒性效应
原理
体外3T3 NRU光毒性测试基于比较化学品在有光照和无光照条件下的细胞毒性:
- 细胞毒性通过中性红(NR)摄取量的浓度依赖性降低来评估
- 中性红(NR)是一种弱阳离子染料,可通过非离子扩散穿透细胞膜并积聚在溶酶体中
- 光毒性机制:光毒剂通过产生活性氧(ROS)等机制导致溶酶体膜通透性增加、pH梯度降低等不可逆变化
- 测试时间:在处理和照射后18-24小时测量NR摄取量
适用范围
适用情况
适用于可能诱导光毒性效应的化学品,包括:
- 局部给药的化妆品成分
- 系统给药后分布到皮肤/眼睛的药物
- 可能暴露于环境光的其他化学品
不适用情况
本测试不设计用于预测:
- 光基因毒性、光过敏、光致癌性
- 间接光毒性机制、代谢产物的效应、混合物的效应
初始考虑和限制
测试方法的主要局限性
UV/vis吸收预筛选要求
关键要求:只有当化学品在290-700 nm范围内具有显著UV/vis吸收时,才应进行光毒性测试。
吸收阈值:摩尔消光系数(MEC)> 1000 L mol⁻¹ cm⁻¹
意义:如果化学品无显著UV/vis吸收,其光激活的可能性极低,预筛选可以避免不必要的动物替代测试。
代谢产物不被测试
本体外测试系统不包含代谢激活系统,化学品的体内代谢产物可能具有光毒性。对于主要经代谢激活产生光毒性的化学品,结果可能为假阴性。
化学品混合物
本方法不适用于化学品混合物,混合物成分可能相互干扰(吸收、淬灭、协同或拮抗作用)。
UV吸收晶体的测试局限性
在测试浓度下形成UV吸收晶体的化学品,晶体沉淀可能导致假阳性或假阴性结果。
水不稳定性化学品
在水溶液中快速降解的化学品可能产生假阴性,测试期间(60分钟处理 + 50分钟照射)的稳定性是关键。
方法选择指导
整合测试策略(IATA)
根据OECD 2024年发布的《光毒性测试整合测试与评估策略指导文件》,建议采用以下分层策略:
第1层:物理化学数据收集
→ UV/vis吸收光谱(290-700 nm)
→ 如MEC < 1000 L mol⁻¹ cm⁻¹,无需进一步测试
第2层:体外光毒性测试
→ 3T3 NRU光毒性测试(本方法)
→ 评估PIF和MPE值
第3层:补充测试(如需要)
→ ROS(活性氧)生成试验
→ 3D皮肤模型测试
→ 其他确认性试验测试流程决策树
测试方法摘要
测试系统
| 组件 | 描述 |
|---|---|
| 细胞系 | BALB/c 3T3(克隆A31)小鼠成纤维细胞 |
| 检测终点 | 中性红(NR)摄取量 |
| 测试条件 | 有光照(+Irr)vs 无光照(-Irr) |
| 照射剂量 | 5 J/cm² UVA(非细胞毒性剂量) |
| 测试时间 | 3天(铺板→处理→检测) |
参考物质
能力验证化学品
| 化学品名称 | CAS号 | 预期PIF | 预期MPE | 光毒性 |
|---|---|---|---|---|
| 胺碘酮盐酸盐 | 19774-82-4 | > 3.25 | 0.27-0.54 | 阳性 |
| 氯丙嗪盐酸盐 | 69-09-0 | > 14.4 | 0.33-0.63 | 阳性 |
| 诺氟沙星 | 70458-96-7 | > 71.6 | 0.34-0.90 | 阳性 |
| 蒽 | 120-12-7 | > 18.5 | 0.19-0.81 | 阳性 |
| 原卟啉IX二钠 | 50865-01-5 | > 45.3 | 0.54-0.74 | 阳性 |
| L-组氨酸 | 70-00-4 | < 1 | 0.05-0.10 | 阴性 |
| 六氯酚 | 70-30-4 | 1.0-1.7 | 0.00-0.05 | 阴性 |
| 十二烷基硫酸钠 | 151-21-3 | 1.0-1.9 | 0.00-0.05 | 阴性 |
推荐常规阳性对照
氯丙嗪(Chlorpromazine, CPZ)是推荐的常规阳性对照物质:
| 参数 | 可接受范围 |
|---|---|
| CPZ (+Irr) IC₅₀ | 0.1 - 2.0 μg/mL |
| CPZ (-Irr) IC₅₀ | 7.0 - 90.0 μg/mL |
| PIF | > 6 |
材料与试剂
细胞系
BALB/c 3T3细胞(克隆A31)
| 属性 | 规格 |
|---|---|
| 细胞类型 | 小鼠成纤维细胞 |
| 克隆 | A31 |
| 物种 | Mus musculus(小鼠) |
| 组织来源 | 胚胎成纤维细胞 |
细胞系来源:必须从认可的细胞库获取
- ATCC:目录号 CCL-163
- ECACC:目录号 93061404
细胞质量控制
支原体检测
- 细胞到达实验室时立即检测
- 仅当检测结果为阴性时才使用
- 之后每3-6个月定期检测
UV敏感性检查
- 对工作细胞库(WCB)至少检查一次
- 在最高使用代次进行测试
- 5 J/cm²剂量下,阳性对照(CPZ)的PIF应 > 6
细胞代次管理
| 细胞库 | 代次范围 | 用途 |
|---|---|---|
| 主细胞库(MCB) | < 20代 | 长期储存,原始来源 |
| 工作细胞库(WCB) | < 40代 | 日常实验的细胞来源 |
| 实验使用 | < 100代(优选< 60代) | 测试用细胞 |
培养基与试剂
完全培养基
| 组分 | 浓度 |
|---|---|
| DMEM | 基础培养基 |
| 新生小牛血清 | 10% (v/v) |
| L-谷氨酰胺 | 4 mM |
| 青霉素 | 100 IU/mL |
| 链霉素 | 100 μg/mL |
培养条件:37°C,5-7.5% CO₂,湿度≥95%
缓冲盐溶液
选择 EBSS(Earle平衡盐溶液)或 HBSS(Hanks平衡盐溶液)
要求:不含蛋白成分、不含光吸收成分(如酚红、维生素)、pH稳定
中性红溶液
工作液配制:50 μg/mL(由 0.5 mg/mL 母液 1:10 稀释)
- 中性红(3-氨基-7-二甲基氨基-2-甲基吩嗪盐酸盐)
- CAS号:553-24-2
- 溶解于无血清培养基
NR提取液(现配)
- 49% 去离子水
- 50% 乙醇
- 1% 冰醋酸
受试化学品制备
溶剂选择(优先顺序)
- 缓冲盐溶液(EBSS/HBSS)
- DMSO - 最高1% (v/v)
- 乙醇 - 最高1% (v/v)
储存
- 测试当天新鲜配制(除非稳定性数据支持)
- 避免预先光激活或降解
仪器设备
细胞培养设备
| 设备 | 规格 |
|---|---|
| CO₂培养箱 | 37°C,5-7.5% CO₂,湿度≥95% |
| 生物安全柜 | II级A2型 |
| 倒置显微镜 | 相差功能 |
| 96孔板 | 无菌、透明底 |
光照系统
光源(太阳模拟器)
推荐类型:
- 氙弧灯 - 与日光匹配最佳
- 掺杂金属卤化物弧灯 - 产热少、成本低
光谱要求:发射完整太阳光谱 290-700 nm,符合ISO D65标准
滤光器
| 滤光器类型 | 特点 | 应用 |
|---|---|---|
| WG320 | 截止波长320 nm | 标准配置 |
| WG335 | 截止波长335 nm | 进一步减少UVB |
| 专用日光滤光器 | 符合ISO D65标准 | 最佳日光模拟 |
剂量测定
UVA计要求:宽带UVA检测器(315-400 nm),定期校准(每年1次)
日常校准步骤:
- 预热光源至少30分钟
- 将UVA计探测器放置在96孔板位置
- 覆盖实际使用的板盖类型
- 记录辐照度读数(mW/cm²)
照射时间计算:
\[ t = \frac{D \times 1000}{I \times 60} \]
其中:\(t\) 为照射时间(分钟),\(D\) 为剂量(J/cm²),\(I\) 为辐照度(mW/cm²)
示例:目标剂量5 J/cm²,测得辐照度1.7 mW/cm²
\[ t = \frac{5 \times 1000}{1.7 \times 60} \approx 49 \text{ 分钟} \]
分析设备
| 设备 | 规格 |
|---|---|
| 酶标仪 | 540±10 nm测量波长 |
| 微孔板振荡器 | 提取NR用 |
| 移液器 | 0.1-1000 μL范围 |
操作步骤
第1天:细胞铺板
制备细胞悬液
- 从工作细胞库复苏细胞或从传代培养中获取细胞
- 用完全培养基调整细胞密度至 1 × 10⁵ cells/mL
- 确保细胞处于对数生长期,活力>90%
铺板
| 板类型 | 孔内容 | 体积 |
|---|---|---|
| 测试化学品板(+Irr) | 100 μL细胞悬液 | 1×10⁴ cells/孔 |
| 测试化学品板(-Irr) | 100 μL细胞悬液 | 1×10⁴ cells/孔 |
| 阳性对照板(+Irr) | 100 μL细胞悬液 | 1×10⁴ cells/孔 |
| 阳性对照板(-Irr) | 100 μL细胞悬液 | 1×10⁴ cells/孔 |
| 周边孔(空白) | 100 μL完全培养基 | - |
要点:每种受试化学品需要2块板(+Irr和-Irr)
培养
将96孔板置于37°C,5-7.5% CO₂培养箱,培养18-24小时,直至形成约50%汇合单分子层。
第2天:化学品处理与照射
制备受试化学品稀释系列
几何稀释系列(8个浓度):
- 最高测试浓度:≤ 1000 μg/mL
- 使用恒定稀释因子(例如:√10或2)
- 保持最终溶剂浓度恒定(通常1% v/v)
处理细胞
- 吸去培养基
- 轻柔洗涤:每孔加入150 μL缓冲液,吸去
- 加入100 μL含相应浓度受试化学品的缓冲液
- 溶剂对照孔:加入含相同浓度溶剂的缓冲液
- 在暗处培养60分钟
光照/避光处理
光照板(+Irr):在室温下通过板盖照射细胞,使用5 J/cm² UVA剂量(约50分钟)
避光板(-Irr):在室温下保持在暗处,时间与照射板相同
洗涤与恢复
- 吸去测试溶液
- 用缓冲液洗涤2次(每孔150 μL)
- 加入100 μL新鲜完全培养基
- 置于培养箱过夜培养(18-24小时)
第3天:中性红摄取测定
显微镜检查
使用相差显微镜检查细胞形态、单分子层完整性、细胞生长状态
中性红摄取
- 预温育缓冲液至37°C
- 吸去培养基,用150 μL温育缓冲液洗涤细胞
- 加入100 μL中性红溶液(50 μg/mL,无血清培养基)
- 在37°C、5-7.5% CO₂条件下培养3小时
洗涤与提取
- 吸去中性红培养基
- 用150 μL缓冲液洗涤细胞
- 吸去缓冲液,彻底去除残留液体
- 加入精确150 μL NR提取液
- 在微孔板振荡器上温和振荡至少10分钟
吸光度测定
在540±10 nm波长下测量吸光度,使用空白孔作为参考。
数据分析
溶剂对照
| 检查项目 | 可接受标准 |
|---|---|
| 照射溶剂对照活力 | ≥ 非照射溶剂对照的80% |
| 溶剂对照OD₅₄₀ | ≥ 0.4 |
| 溶剂对照PIF | < 2 |
阳性对照(氯丙嗪,CPZ)
| 检查项目 | 可接受范围 |
|---|---|
| CPZ IC₅₀(+Irr) | 0.1 - 2.0 μg/mL |
| CPZ IC₅₀(-Irr) | 7.0 - 90.0 μg/mL |
| CPZ PIF | > 6 |
数据点要求
- 至少8个浓度点
- 覆盖完整的浓度-响应关系
- 包括在50%活力上下的浓度点
细胞活力计算
\[ 相对活力(\%) = \frac{OD_{测试} - OD_{空白}}{OD_{溶剂对照} - OD_{空白}} \times 100 \]
光毒性指标计算
光刺激因子(PIF)
\[ PIF = \frac{IC_{50}(-Irr)}{IC_{50}(+Irr)} \]
- IC₅₀(-Irr):无光照条件下使活力降低50%的浓度
- IC₅₀(+Irr):有光照条件下使活力降低50%的浓度
特殊情况:如果一个化合物光照有细胞毒性,而无光照情况下无细胞毒性,可使用:
\[ PIF = \frac{C_{max}(-Irr)}{IC_{50}(+Irr)} \]
如果化合物在有光照和无光照都不表现为细胞毒性,则PIF = 1
平均光效应(MPE)
\[ MPE = \frac{\sum_{i=1}^{n} w_i \cdot PE_{c_i}}{\sum_{i=1}^{n} w_i} \]
其中:
- \(PE_c = RE_c \times DE_c\)(光效应)
- \(RE_c = R_c(-Irr) - R_c(+Irr)\)(响应效应)
- \(DE_c = \frac{C/C^*-1}{C/C^*+1}\)(剂量效应)
- \(w_i = \max\{R_i(+Irr), R_i(-Irr)\}\)(权重因子)
软件工具
PhotoTox version 2.0:OECD秘书处提供PIF和MPE计算软件包
下载地址:https://www.oecd.org/en/topics/sub-issues/testing-of-chemicals/software-test-guidelines.html
软件安装与使用
仅支持Windows系统,运行 Setup.exe 安装。
新建项目
点击 File → New 或按 Ctrl+N
输入数据
选择 select source file 导入数据,只能接受96孔板布局的 txt 文件。
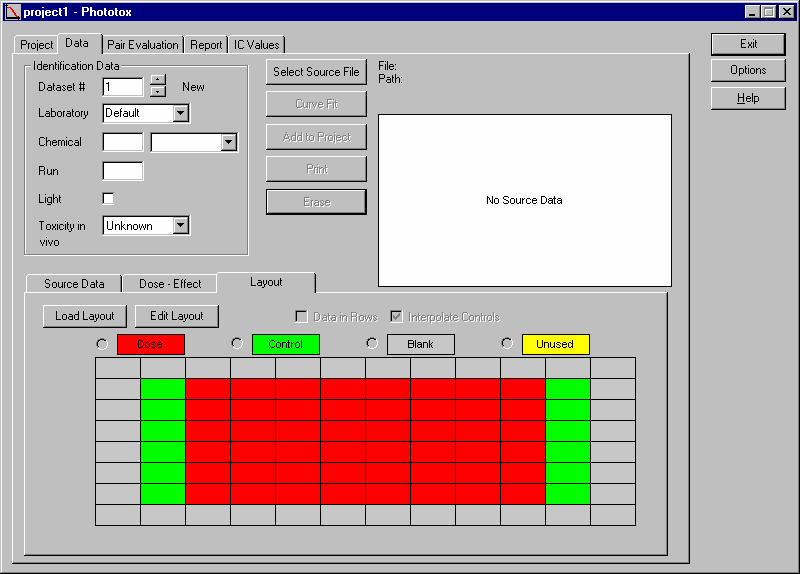
板子布局
在Layout中可编辑布局,手动输入检测样品的浓度(最少8个样品)。
拟合曲线
输入浓度和数据后,点击 curve fit 进行拟合。
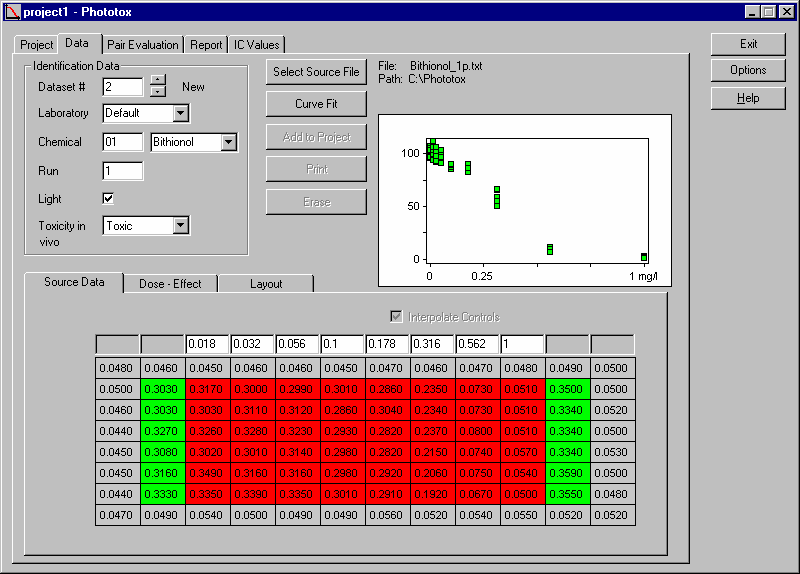
每次拟合后点击 Add to project,否则数据会被覆盖。
计算
将 +UV 和 -UV 数据拟合后添加到项目,打开 “Pair Evaluation” 计算 PIF 和 MPE。
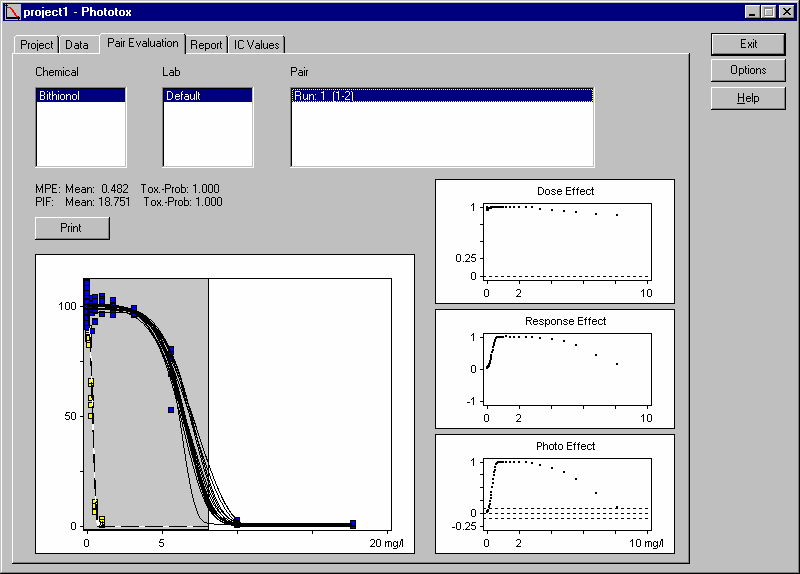
结果解释
判读标准
| PIF | MPE | 预测结果 |
|---|---|---|
| < 2 | < 0.1 | 无光毒性 |
| ≥ 2 且 < 5 | ≥ 0.1 且 < 0.15 | 可疑光毒性 |
| ≥ 5 | ≥ 0.15 | 光毒性 |
重要说明:PIF和MPE应同时考虑。如不一致,采取保守方法归类为”可疑光毒性”。
特殊情况处理
仅在最高浓度观察到光毒性
- 检查实验充分性(是否达到最大可行浓度)
- 评估暴露相关性(是否有皮肤吸收数据)
- 考虑补充测试(ROS试验、3D皮肤模型等)
可疑/边界结果
- 首先检查测试质量
- 考虑重复测试或调整实验参数
- 进行确认性测试
PIF无法计算
- 使用MPE指标
- 评估是否在最高浓度观察到显著差异(> 20%活力差异)
质量控制
细胞质量控制
- 支原体检测:细胞到达实验室时检测,仅当阴性时使用
- UV敏感性检查:对工作细胞库至少检查一次
- 历史数据:建立阳性对照的MPE历史数据库
仪器质量控制
- 光源:每次测试前检查辐照强度
- 培养箱:每日记录温度和CO₂浓度
- 酶标仪:定期校准波长和吸光度准确性
测试报告
测试报告应包括以下信息:
受试化学品
- 识别数据、通用名、IUPAC名和CAS号
- 物理性质和纯度
- UV/vis吸收光谱
- 稳定性和光稳定性
溶剂
- 选择理由
- 受试化学品在溶剂中的溶解度
- 处理培养基中溶剂的百分比
细胞
- 细胞类型和来源
- 无支原体和其他污染
- 细胞传代代次
- 辐射敏感性
测试条件
- 培养基类型和组成
- 培养条件(CO₂浓度、温度、湿度)
- 化学品处理持续时间
- 照射参数(光源、滤光器、UVA剂量)
- 中性红活力测试条件
结果
- 各浓度下的细胞活力
- 浓度-响应曲线
- IC₅₀值和PIF/MPE
- 测试接受标准
附录
附录A:测试流程图
flowchart TD
A[第1天:细胞铺板] --> B[18-24 h培养<br/>形成50%汇合单层]
B --> C[第2天:化学品处理]
C --> D[60分钟暗培养]
D --> E{分板}
E --> F[+Irr板:5 J/cm² UVA照射]
E --> G[-Irr板:暗处50分钟]
F --> H[洗涤 + 新鲜培养基]
G --> H
H --> I[18-24 h恢复培养]
I --> J[第3天:中性红摄取测定]
J --> K[3小时NR培养]
K --> L[提取 + 测定OD540]
L --> M[数据分析:计算PIF/MPE]
M --> N[结果判读]
附录B:决策树
flowchart TD
A[评估化学品物理化学性质] --> B{UV/vis吸收光谱}
B -->|MEC < 1000 L mol⁻¹ cm⁻¹| C[无需光毒性测试]
B -->|MEC > 1000 L mol⁻¹ cm⁻¹| D[体外3T3 NRU光毒性测试]
D --> E{PIF < 2 或 MPE < 0.1}
E -->|是| F[无光毒性]
E -->|否| G{PIF > 5 或 MPE > 0.15}
G -->|是| H[光毒性]
G -->|否| I[可疑光毒性<br/>需进一步评估]
附录C:PIF和MPE计算示例
示例:使用PIF判断
原始数据:
| 浓度(μg/mL) | OD540 (+Irr) | OD540 (-Irr) |
|---|---|---|
| 0(溶剂对照) | 1.20 | 1.18 |
| 0.1 | 1.15 | 1.16 |
| 0.3 | 0.95 | 1.12 |
| 1.0 | 0.60 | 1.05 |
| 3.0 | 0.25 | 0.85 |
| 10.0 | 0.10 | 0.55 |
| 30.0 | 0.05 | 0.30 |
计算步骤:
- 通过非线性回归确定IC₅₀:IC₅₀(+Irr) = 1.8 μg/mL,IC₅₀(-Irr) = 28.5 μg/mL
- 计算PIF:PIF = 28.5 / 1.8 = 15.8
- 判断:PIF > 5 → 光毒性阳性
附录D:验证研究数据摘要
实验室间验证研究(1996-1998)
参与实验室:11个欧洲实验室
测试化学品:20种
| 统计指标 | 结果 |
|---|---|
| 敏感性 | 100% (10/10) |
| 特异性 | 80% (8/10) |
| 准确率 | 90% (18/20) |
附录E:阳性对照试剂准备
氯丙嗪储液制备(1 mg/mL,在DMSO中):
- 精确称取10 mg氯丙嗪
- 加入10 mL DMSO
- 涡旋混合直至完全溶解
- 分装至小体积,避光保存于-20°C
工作液制备:在EBSS/HBSS中稀释至所需浓度范围,保持最终DMSO浓度恒定为1% (v/v)